研究内容 | |||
| 目標:
(1) 生理活性脂質、特にスフィンゴシン1-リン酸(S1P)、リゾホスファチジン酸(LPA)の作用機構の解明とそれに関連した薬剤の開発。 (2) 細胞外pH(プロトン)を感知する新しいG蛋白連関受容体の生理的ならびに病態生理学的な役割に関して、特に中枢神経系、骨代謝、炎症性疾患に焦点をあて解明する。 | |||
|
| |||
 |
 |
 |
 |
|
|
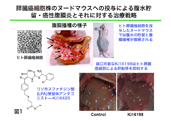
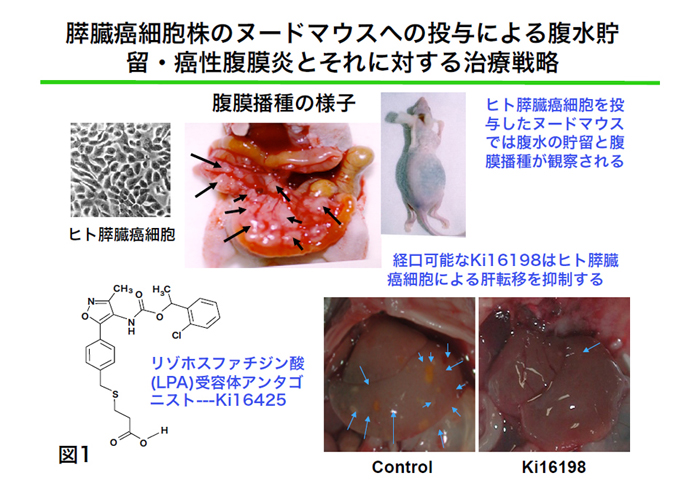
スフィンゴシン1-リン酸(S1P)やリゾホスファチジン酸(LPA)などの脂質性 メディエーターは細胞膜受容体を介して細胞増殖、遊走、アポトーシスなどさ まざまな細胞機能に関わっている。現在、これらの受容体としてS1P1〜5、LPA1 〜6が知られている。我々はLPA受容体拮抗薬Ki16425の作用機序を明らか にした。この薬剤は基礎研究、また、各種病態たとえば、癌(膵臓癌、グリオー マ)、慢性リウマチ、動脈硬化症などの治療薬としても期待される(図1)。 (1) S1P結合蛋白質アポリポプロテインMのS1P産生における役割 |
 |
|
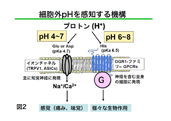
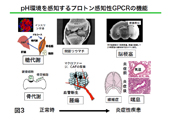
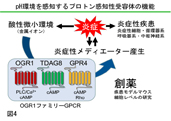
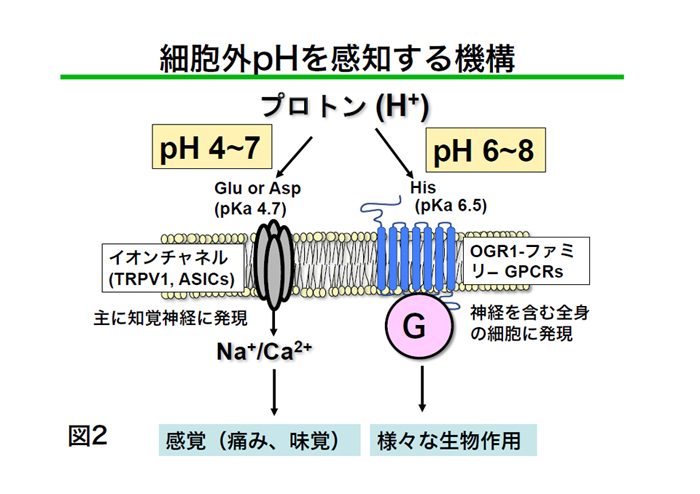
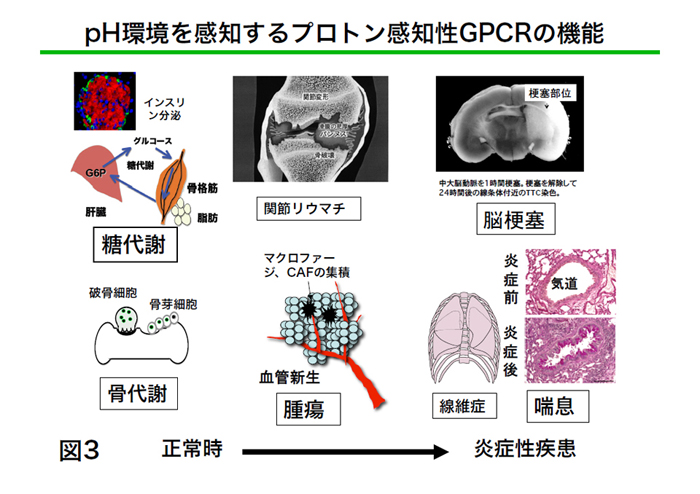
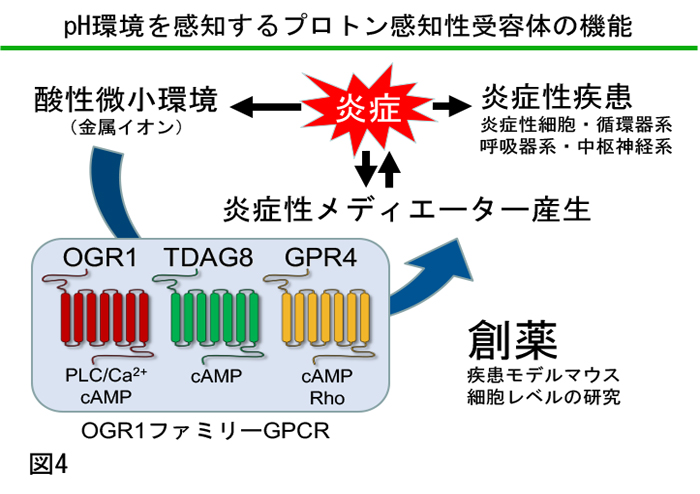
リゾ脂質性メディエーター受容体として同定されていたG蛋白質共役受容体 (GPCR)が細胞外のpHを感知することを見いだした。従来から知られているプ ロトン感知機構としてはTRPV1等のチャネル機構が知られている。これらのチ ャネルはpH4〜6(TRPV1)、pH4〜7 (ASICs)のプロトン濃度をチャンネル分子上 のグルタミン酸やアスパラギン酸残基が感知し、痛み、味覚など感覚神経で主 に働いている。一方、OGR1ファミリーGPCRは受容体上のヒスチジン残基が pH6〜8のより生理的なプロトンを感知し、神経細胞も含めた様々な細胞に発現 している(図2)。細胞外プロトンは生理的な状態でも40 nM (pH 7.4) 存在し、 腫瘍、虚血や炎症部位では1000 nM (pH6.0)にも増加する。この受容体の生理機 能と病態との関連について、中枢神経系、骨代謝、炎症性疾患を中心にsiRNA によるノックダウン細胞、ノックアウトマウスを用いて解析している(図3)。 (1) ミクログリアや神経細胞におけるプロトン感知性GPCRの役割 |
 |
 |
 |